對于藥品質量標準的內容,從事分析工作的同學再熟悉不過,性狀、鑒別、檢查、含量測定。其中檢查項基本可分為安全性檢查和有效性檢查。有效性檢查項目包括大家熟知的裝量差異、溶出度、含量均勻度、可見異物、不溶性微粒、水分、有關物質等等......微生物限度檢查和無菌檢查則屬于安全性檢查的部分。安全性檢查是比有效性檢查的項目更加需要關注和嚴格制定的。
今天小編就帶大家重點學習微生物限度檢查和無菌檢查。1.什么情況下質量標準中該制定微生物限度?2.什么情況下該制定無菌檢查?3.限度又該如何確定?
什么是無菌檢查?
無菌檢查法系用于檢查藥典要求無菌的藥品、生物制品、醫療器具、原料、輔料及其他品種是否無菌的一種方法。
限度制定
1、制劑通則或品種項下要求無菌及標示無菌的制劑和原輔料應制定無菌限度。包括注射劑、眼用制劑、吸入液體制劑、沖洗劑等。
2、用于手術、嚴重燒傷、嚴重創傷的局部給藥制劑。
檢查方法
無菌檢查法包括薄膜過濾法和直接接種法。只要供試品性質允許,應采用薄膜過濾法。
薄膜過濾法一般應采用封閉式薄膜過濾器。無菌檢查用的濾膜孔徑應不大于0.45微米 ,直徑約為50mm。根據供試品及其溶劑的特性選擇濾膜材質。使用時,應保證濾膜在過濾前后的完整性。
直接接種法適用于無法用薄膜過濾法進行無菌檢查的供試品,即取規定量供試品分別等量接種至硫乙醇酸鹽流體培養基和胰酪大豆胨液體培養基中。

什么是微生物限度檢查?
藥典中常見的格式:
微生物限度 取本品,照非無菌產品微生物限度檢查:微生物計數法(通則1105)和控制菌檢查法(通則1106)及非無菌藥品微生物限度標準(通則1107)檢查,應符合規定。
微生物限度檢查法系檢查非規定滅菌制劑及其原料、輔料受微生物污染程度的方法。
檢查項目包括需氧菌總數、霉菌和酵母菌總數及控制菌檢查。
微生物計數法:用于能在有氧條件下生長的嗜溫細菌和真菌的計數。
控制菌檢查根據藥物劑型的不同,包括大腸埃希菌、耐膽鹽革蘭氏陰性菌、沙門菌、銅綠假單胞菌、金黃色葡萄球菌、梭菌、白色念珠菌。
結果判斷
需氧菌總數指TSA培養基上生長的總菌落數,霉菌和酵母菌總數指SDA培養基上生長的總菌落數。
控制菌檢查則以陽性對照試驗檢出相應控制菌、陰性對照試驗無菌生長下,供試品檢查的結果為準。

限度制定
微生物限度的制定,根據制劑、原料、中藥提取物的不同,標準會有不同:
第一種情況
如果制劑是非無菌化學藥品制劑、或生物制品制劑、或不含藥材原粉的中藥制劑,請看表1的限度標準。
控制菌檢查法:用于在規定的試驗條件下,檢查供試品中是否存在特定的微生物。
微生物計數法的供試品檢查包括三種方法:平皿法、薄膜過濾法、MPN法,都是根據計數方法適用性試驗確定的。

舉個例子,如阿司匹林腸溶片。
首先,判斷其分類屬于口服給藥的固體制劑。
其次,在上表中找到其所屬分類(第一列第二行)。
則其應遵守的限度標準如下:需氧菌總數的限度應是10^3,即2000cfu/g;霉菌和酵母菌總數的限度是10^2,即200cfu/g;不得檢出大腸埃希菌(1g或1ml),含臟器提取物的制劑還不得檢出沙門菌(10g或10ml)。標準的一些說明:
2015版《中國藥典》四部通則1107中關于菌數標準的解釋 。
根據藥典中大腸埃希菌的檢查方法,表1中的"控制菌"項下的要求才被規定為“不得檢出大腸埃希菌(1g或1ml)”。
同理適用于沙門菌的檢驗,表1中的"控制菌"項下的要求規定為“含臟器提取物的制劑還不得檢出沙門菌(10g或10ml)”。
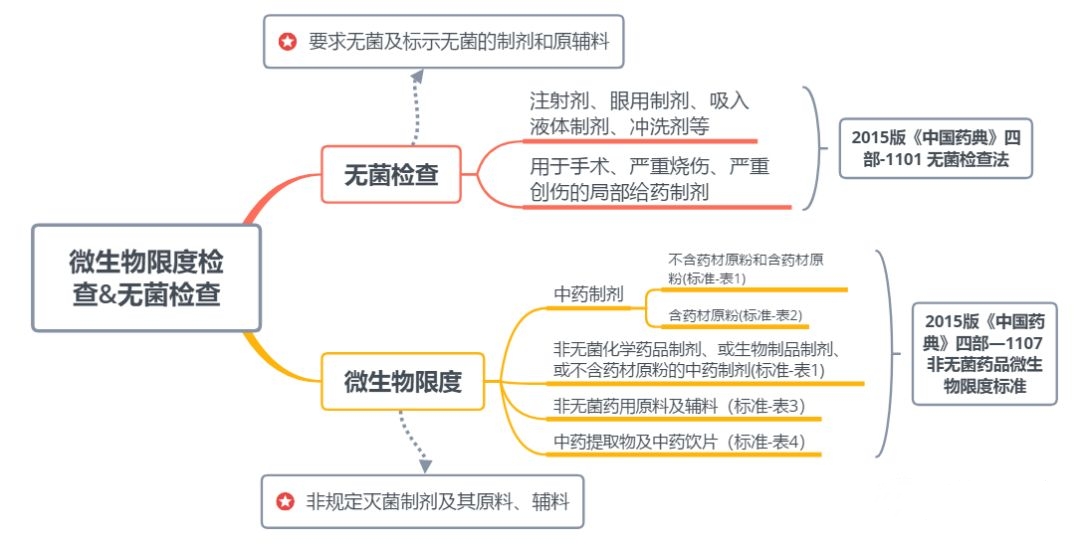
第二種情況
如果你做的是中藥制劑,就分為兩種情況:不含藥材原粉和含藥材原粉
看完上述講解后,我們再看一遍開篇的示例,是不是能很好理解了?
隨便選一個藥品原料、輔料、制劑,該做無菌?該做微生物限度?做哪方面內容?各自限度是什么?都能回答出來了吧?







 客服1
客服1